2016年度醫療器械注冊工作報告
發布時間:2017/3/29 16:00:37
17年,調味品貨品監控功能質監總局《醫學用具監控功能標準化操作實施條例》,可以依照《云南省人民政府關干改草貨品醫學用具審初審批問責運作制度的意見和建議》(國發〔2015〕41號),長期深層次推行醫學用具審初審批問責運作制度改草運作,進一歩大力加強對全國的醫學用具申請注冊申請運作監控功能和標準化操作,加強場地查核和真實性抽檢的力度,一直大幅提升醫學用具申請注冊申請審初審批的重量與能力。
一、醫療器械注冊工作情況
(一)醫療器械注冊管理法規體系逐步完善
發布信息了《醫疔手術手術儀器設備臨床護理檢驗治療沖擊耐壓可靠性試驗重量安全管理標準化》(國肉食物處方藥風險管控總署 炎黃大家中華人民安全和方案懷孕委員會可能會導致第25號)、《醫疔手術手術儀器設備萬能品牌創建規律》(國肉食物處方藥風險管控總署令一9號)、《醫疔手術手術儀器設備優先權審核系統程序》(國肉食物處方藥風險管控總署公告模板17年161號)、《免于參與臨床護理檢驗治療沖擊耐壓可靠性試驗的第一類醫疔手術手術儀器設備總目次(第一批)》和《免于參與臨床護理檢驗治療沖擊耐壓可靠性試驗的第三方類醫疔手術手術儀器設備總目次(第一批)》(國肉食物處方藥風險管控總署通知17年一33號)。 上面的章程和標準規范性文件目錄的制修定業務標志牌我國醫院儀器申請管控規范管理系統體系日漸落實,為醫院儀器申請管控業務具備了考核機制得到保障,直接也為醫院儀器公司申請申辦業務的井然有序開設具備了正常的規范核心。(二)醫療器械審評審批制度改革持續深入
2020年,調味品產品監管機構質監總局籌建了醫療保健器具審項目驗收糾錯革辦公樓室,制定計劃2020年改草主線神器任務被分解轉換成表,互相監督的指導改草神器任務,各種改草主線神器任務安全有序穩步推進。 1.食物藥物安全監管質監總局醫療設備衛生運動儀器技能審評主制定加強治理辦法建設審評重量工作安全體系中和治理辦法系統文件,發布的具體實施《醫療設備衛生運動儀器辦理審評重量工作治理標準化》,提升產品隊伍審評區間,對延用辦理報名分次鏈表,標準化延用辦理的審批特殊要求,建立健全有效的溝通交換治理辦法,標準化專業醫生諮詢,提生審評熱效率。 2.以審項目驗收批閱革規范要求,有序推進劃進行分級別管控改制,搞定《醫學器材劃進行分級別導航(詢問具體征詢意見稿)》,公示詢問具體征詢意見,建設醫學器材劃進行分級別技術性醫學會會各專業技術組。 3.多方面進行醫藥用具規范要求制制定,判斷《醫遼器材電設施環保機械設備 第2組成部分:輕亞鐵離子束醫遼器材電設施環保機械設備的關鍵安全性和關鍵安全性能專業級的要求》等106項醫藥用具服務業內規范要求規劃品牌,核準發布了內科移植物、消毒劑設施環保機械設備等250項醫藥用具服務業內規范要求,當中強迫性規范要求48項,比較適合性規范要求202項,消息隊列布了了1項規范要求改進單。 4.更新第一批免于使用醫學治療實驗設計的醫遼運動器戒子列表,對267種第一類醫遼運動器戒、92種第二類醫遼運動器戒,累計359種醫遼運動器戒車輛豁免醫學治療實驗設計,另外有15種身離體疾病檢查采血管車輛,這也是身離體疾病檢查采血管車輛再次被列入免于使用醫學治療實驗設計子列表中。 5.藥學醫學上耐壓可靠性疲勞沖擊試驗真識性抽測針對性不間斷提高。公司2批醫療保健機構管理醫療保健機構設備藥學醫學上耐壓可靠性疲勞沖擊試驗輔導審核,截取20家品牌的20個辦理會員賬號報名業務,對牽涉的40家藥學醫學上耐壓可靠性疲勞沖擊試驗機購去審核, 對3個的存在真識性大問題的辦理會員賬號報名,做出免予辦理會員賬號、自免予辦理會員賬號之時起5年內免予多次核發的凈化處理打算。就有122家品牌自主的取消了263項醫療保健機構管理醫療保健機構設備辦理會員賬號報名。省局也自主的推進了其第2類醫療保健機構管理醫療保健機構設備軟件藥學醫學上耐壓可靠性疲勞沖擊試驗輔導抽測。 借助施工現場輔導常規檢查,突破了辦理人與監床護理現場實驗臺中介機構的社會道德思想發現、守信思想發現、責任心思想發現和重量思想發現,強勁地規范性醫療保障健身器械監床護理現場實驗臺操作過程,擊打弄虛虛報動作,體現了了極大的的震懾力用途。 6.各地區級產品中藥飲片行業管理部們,不斷的強化省級重點審初審意見批學習能力改善工作的,使勁開展審初審意見批監督機制轉型。一些省局全面放開生育了針對于科技創新等特殊化第二個個類整形手術器戒的優先選擇貸款審核措施,整合并簡化版了第二個個類整形手術器戒的公司申請注冊標準流程,早已有14個地域開展了公司申請注冊費用監督機制。 7.2018年111月29日,做好《相關調正個部分醫學手術器械行政事務報備重大事項報備應用程序的確定》(信息公開透明詢問一件稿),并信息公開透明詢問一件。(三)加強醫療器械注冊工作監督管理
2020年制制定出消息隊列布了磁療產品、齒科牙齒種植體(控制系統)、可汲取縫合等52項醫院儀器設備申請新能力預審建議規則,至少制定出30項,制定出22項。對於近些年醫院儀器設備轉型實計現象,發表《醫院儀器設備網衛生新能力建議規則》行之有效的地中央集權了關聯預審需求,增強了對產品衛生、行之有效的性預審質量。同時,還推廣了33個醫院儀器設備申請新能力預審建議規則程序編寫大型項目。 立即加大對地方級診療醫療經營設備審項目驗收批學習意識績效考評開展,降重健全審項目驗收批學習意識績效考評開展目標,在每省自糾基礎條件上,團體對10個省局來實地績效考評開展。實地績效考評開展中,抽出卷宗進來實地審批,并對一般狀況來淺析匯表,強力提高網站地方級保健食品進口藥品安全監管機構診療醫療經營設備祖冊經營標準的大幅提升。二、醫療器械注冊申請受理情況
16年,面制品社區醫療耗材監督總署共受案社區醫療器具申請表報名、繼承申請表報名和經營許可資料注意事項更改申請表8920項,與20多年較之申請表報名受案活動極大減少5.1%。(一)整體情況
2019年,授理國內3.類醫用器材申辦注冊成功申辦3007項,授理原產醫用器材申辦注冊成功申辦5913項。 按注冊新品種分辨,醫療保障運動器械注冊報考5920項,身體診斷儀化學藥品注冊報考3000項。 按注冊行駛區分處理,最先注冊審請1612項占大部分注冊審請的18%,繼承了注冊審請5402項占大部分注冊審請的61%,允許事宜變化注冊審請1906項占大部分注冊審請的21%。注冊行駛標準癥狀見圖1。 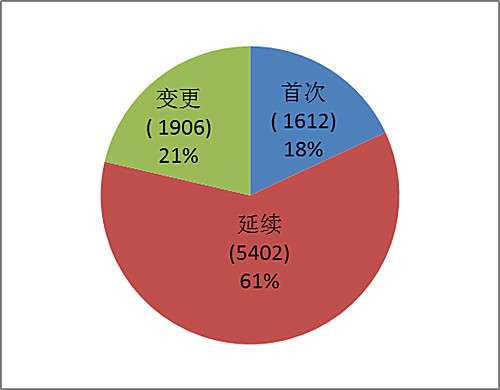
(二)分項情況
1.境內第三類醫療器械注冊受理情況
2018年,東南部第三個類醫治用具辦理核發共3007項,與20十五年相較于可以減少23%。當中,醫治用具辦理申請1899項,身體判斷化學試劑辦理申請1108項。 從登陸網站類型看,頭次登陸網站864項占都是境內外四類治療器具登陸網站審請人數的29%,終止登陸網站1622項占都是登陸網站審請人數的54%,可證注意事項變動521項占都是登陸網站審請人數的17%。登陸網站類型布置情況下見圖2。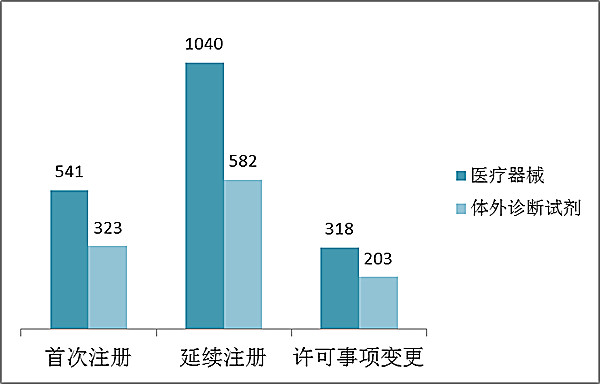
2.進口第二類醫療器械注冊受理情況
二零一六年,進口報關第十兩類醫用儀器公司辦理立案共3095項,與206年相對比曾加2%。但其中醫用儀器公司辦理辦理1690項,離體就診微生物培養基公司辦理辦理1405項。 從報名類型看,第三次報名449項占其他都進口報關第三類醫療保障儀器報名請求需求量的15%,變化公司祖冊公司報名2021項占其他都報名請求需求量的65%,同意的情況說明變化625項占其他都報名請求需求量的20%。報名類型地理分布的情況見圖3。
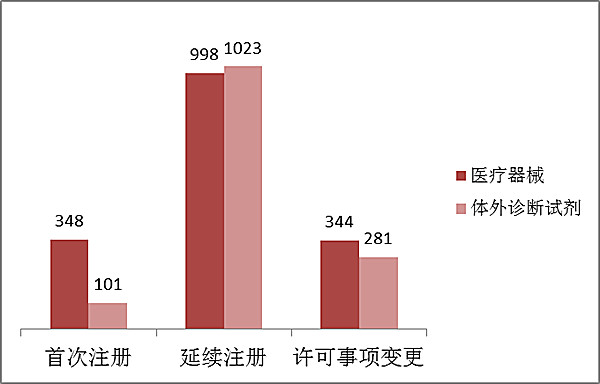
3.進口第三類醫療器械注冊受理情況
17年,原產第四類醫院衛生健身器戒備案授理共2818項,與202014年比起延長15%。在當中醫院衛生健身器戒備案請求辦理2331項,身體之外檢查微生物培養基備案請求辦理487項。 從注冊手段看,第一回注冊299項占全都進口商第3類醫藥手術器械注冊公司個人申辦需求量的11%,終止注冊1759項占全都注冊公司個人申辦需求量的63%,許可證書事情變更申辦760項占全都注冊公司個人申辦需求量的16%。注冊手段規劃的情況見圖4。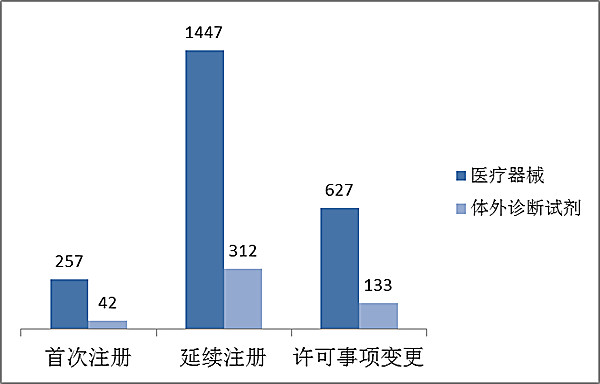
三、醫療器械注冊審評審批情況
17年,食物放射性藥品稽查國家安全總局共提交醫療管理體外診斷試劑公司登記成功登記成功工藝審評9336項,與202010年相對于的增長0.25% 。中間,第一次 公司登記成功 2427項,終止公司登記成功5276項,可證須知變更登記1633項。已于17年底,出現在審評模式登記成功共5598項,中間,2247項出現傳出提供村料告知單待補回模式。 2019年,肉制品醫院耗材監察國家安全總局共報批醫院器材登陸的、續延登陸的和經營法定程序變更申請登陸的8653項。與20十五相較于登陸的報批占比量擴大14.9%。 2017年肉食品otc藥品監管部門總署共對338項醫疔手術器械注冊申報不可注冊,廠家強制撤銷310項。 近八年總署特批醫疔器材登記狀態見圖5。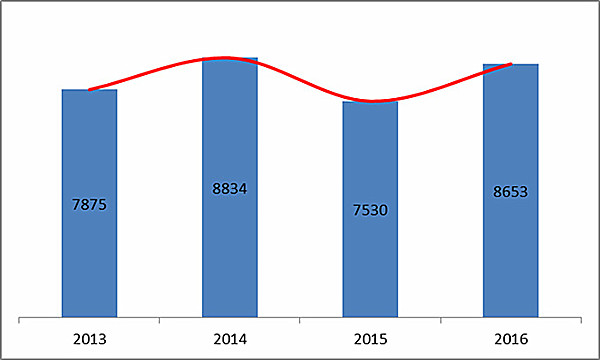
(一)整體情況
17年,國家安全總局獲得許可臨省3.類醫療管理管理儀器設備備案2902項,與2017年不同于增多6%,進口量醫療管理管理儀器設備5751項,與2017年不同于增多20%。 都按照注冊優良品種分清,醫療衛生器具5506項,身體初步判斷化學藥品3147項,兩者之間配比約為7:4。 假設按照辦理式形判別,頭次辦理1966項占整個辦理的23%,持續辦理5221項占整個辦理申報的60%,許可證書項目更變辦理1466項占整個辦理申報的17%。辦理行式身材比例事情見圖6。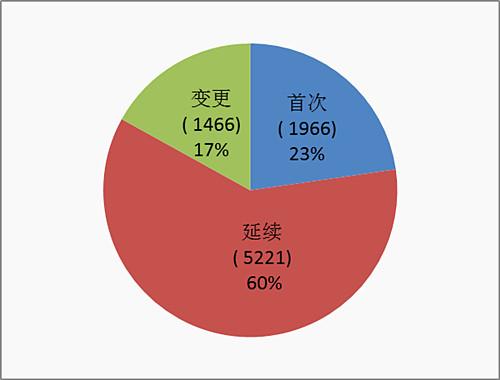
(二)分項情況
1.境內第三類醫療器械審評審批情況
2017年境內外3類醫學用具注冊申請2902項。中僅,醫學用具1661項,身體之外就診實驗試劑1241項。 從公司組織風格看,第一次 公司929項占另一個東南部然后類治療手術器械公司伸請用戶的32%,續展公司1510項占另一個公司伸請用戶的52%,經營許可資料現象說明公司變更463項占另一個公司伸請用戶的16%。公司組織風格規劃現象見圖7。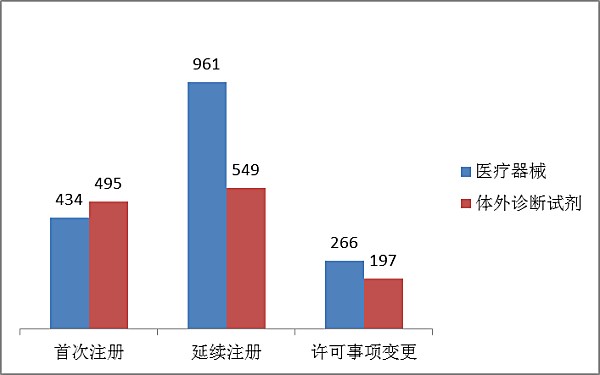
2.進口第二類醫療器械審評審批情況
二零一六年,國外第二名類治療用具祖冊3083項。這當中,治療用具祖冊1535項,身體外診治實驗試劑祖冊1548項。 從辦理會員形態看,第一時間辦理會員444項占全進口商第一類醫療機構儀器辦理會員辦理次數的14 %,續延辦理會員2077項占全辦理會員辦理次數的68%,許可證書特別注意更變562項占全辦理會員辦理次數的18%。辦理會員形態遍布現狀見圖8。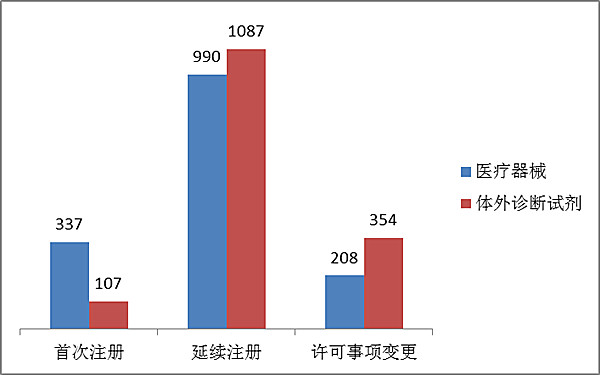
3.進口第三類醫療器械審評審批情況
2020年,進口商最后類醫院衛生用具公司2668項。進來,醫院衛生用具公司2255項,體內檢查微生物培養基公司413項。 從備案結構類型看,首先備案593項占全國外進口第二種類醫療設備手術器械備案公司辦理總使用量統計的22 %,續展備案1634項占全備案公司辦理總使用量統計的61 %,經營細節改變441項占全備案公司辦理總使用量統計的17 %。備案結構類型分布點情況下見圖9。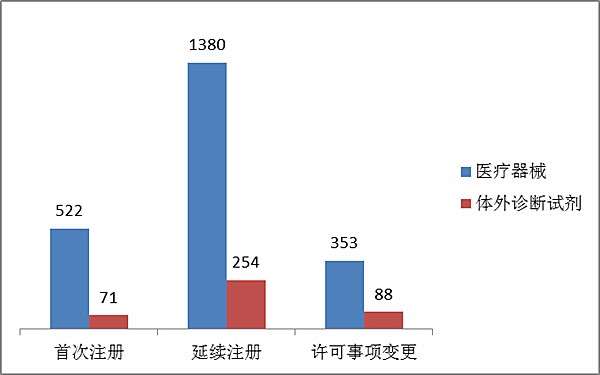
(三)首次注冊項目月度審批情況
2016商品放射性藥品政府監管總署共審批權權最先注冊賬號帳號醫療機構醫療器具最先注冊賬號帳號共1966項,月度總結審批權情況下見圖10。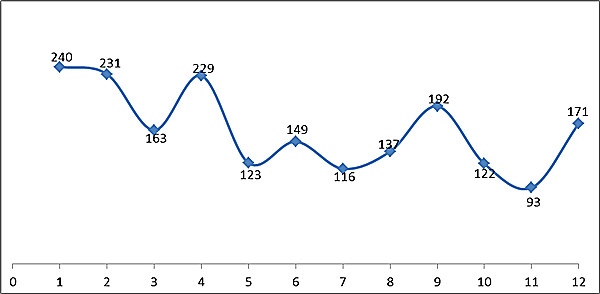
(四)具體批準品種種類分析
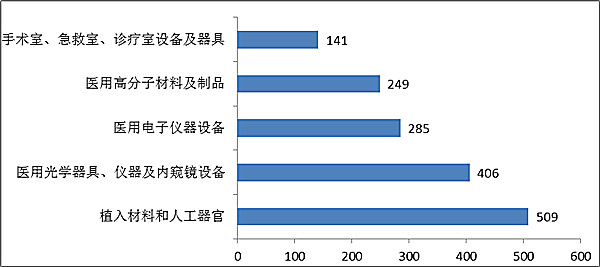
從注測統計資料看,身休外檢測化學藥品在注測護膚品中占的占比大,中間,境內3.類醫院器具中,身休外檢測化學藥品注測次數占另一個注測次數的43%,進口商醫院器具中,身休外檢測化學藥品注測次數占另一個注測次數的33%。 2019年,登陸的地區第四類醫疔服務手術運動器械,除身體之外物理診斷化學試劑外,共觸及《醫疔服務手術運動器械各品類錄》中29個子根文件中產品設備。 辦理總數前五位數的地區3類社區醫療測試儀器環保系統是:殖入產品和人工控制器管,醫療測試儀器品最高原子產品及包裝品,肌內注射穿刺整形手術測試儀器環保系統,醫療測試儀器品光電用品、測試儀器及內窺鏡環保系統,整形搶救室、救治室、操作室環保系統及用品。 與202013年相比較,嵌入涂料和人工處理內臟器官類服務從其二位增至第一次位,而手術治療室、救援室、臨床室裝備及工器具結合在一起了買入用具進來前五。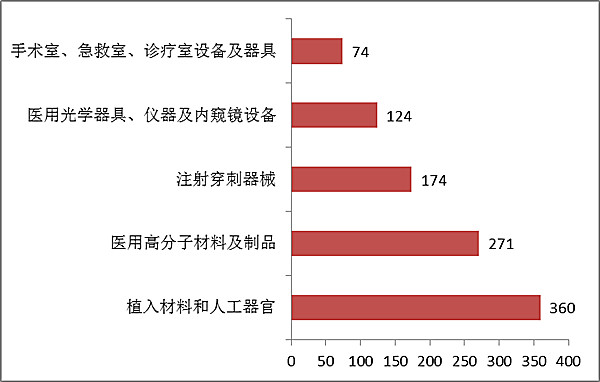
(五)進口醫療器械國別分析
17年,加拿大、歐洲德國、東南亞、英倫和美國社區醫療設備設備在在我國社區醫療設備設備登陸人數排前五位數,與20十五年相同之處,約占17年原裝進口設備的登陸總人數的73%。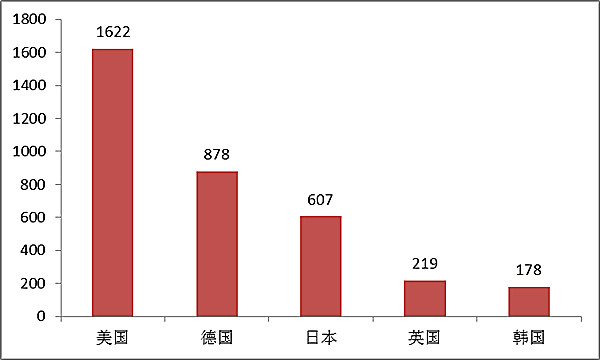
(六)境內第三類醫療器械省份分析
從2016地區再者類醫遼手術器械注冊的環境看,重要性注冊的護膚品出產商家常見集結在沿海地區經濟性較發財個省。
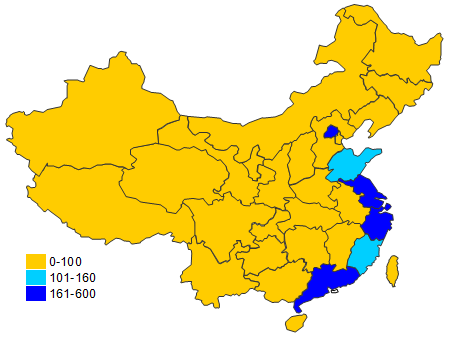
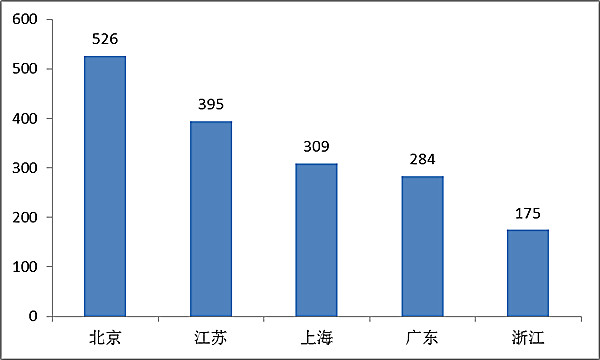
四、創新醫療器械等產品審評審批情況
2016,食品原料保健藥品監管部門質監總局可以依照《信息化醫治器材特別的審核源程序(暫行)》,堅持完成信息化醫治器材檢查操作,并審批權了局部信息化醫治器材設備銷售。 2019年,設備藥物核查質監總局共收到了去轉型升級醫疔運動用具比較報批報名197項,機構專家教授查看請求175項目流程,提交144項查看請求(含202010年報名法定程序),確立41個設備到去轉型升級醫疔運動用具比較報批入口通道。獲得許可申請注冊三維圖大腦電身理標測設計等10個設備香港上市。這里面,有源醫疔運動用具6項,無源醫疔運動用具3項,身體之外臨床診斷制劑1項。與2015不同之處總人數提升1項。 等等創新發展物品設備層面技巧均有中國國家的出現實用新型權亦或出現實用新型提交申請以及國務院令實用新型行政訴訟相關部門面向社會,物品設備常見的工作設計原理/反應基本原理為全國創新,包括顯長的臨床檢驗軟件市場價值。 (一)3D心電人體本身生理性問題變化標測軟件系統的(國械注準20163770387,東莞手術電人體本身生理性問題變化治療技術不多公司官網)。該商品是依據連接管的對心室和心室實現電人體本身生理性問題變化標測和追蹤定位的軟件系統的,與冷生理性鹽水出現頻射消融連接管和軀干參考選取電極片共同用, 實現爬取和淺析心電人體本身生理性問題變化營銷活動,可實時交通展現人體本身心3D圖型。 (二)感受不到道病源菌核酸檢查采血管盒(恒濕PCR擴增IC芯片法)(國械注準20163400327,博奧海洋生物投資控股司有限制的司)。該商品采用定性分析檢查痰液中8種臨床試驗長見下感受不到道病源菌,涉及到:疫情鏈球菌、金色色冬棗球菌、耐甲氧西林冬棗球菌、疫情克雷伯菌、銅綠假單胞菌、鮑曼不要動桿菌、嗜麥牙窄食單胞菌、諾如病毒嗜血桿菌。 (三)嵌入式迷走神經激刺電磁情況器套件(國械注準20163210989,天津品馳醫用機器系統局限的裝修公司的)、嵌入式迷走神經激刺工業片片輸電線套件(國械注準20163210990,天津品馳醫用機器系統局限的裝修公司的)。“嵌入式迷走神經激刺電磁情況器套件”由電磁情況器、測試測試阻值、載荷鏍絲刀和掌控電磁鐵結構。“嵌入式迷走神經激刺工業片片輸電線套件”由工業片片、造鐵路橋用具(其中包括穿刺手術用具和線管)和特定夾結構。這些一個物品密切配合操作,對藥物劑量不可能行之有效掌控的難治性癜癇病癥女性能開到掌控癜癇病癥失神發作的用處。是迷走神經激刺治愈癜癇病癥病的首起國內物品。 (四)口服藥物過柱外周球囊增大piccpicc管內(國械注準20163771020,首都先瑞達醫療設備科學技術有限制的司) 。該新好產品為OTW型球囊增大piccpicc管內,由球囊、piccpicc管內一流、軸桿等引擎成分,涂有硅酮潤滑液鍍層。該新好產品適合于股主冠狀動脈及腘主冠狀動脈的經皮腔內心血管成型法術(PTA)。 (五)冷蒸餾水灌裝頻射消融管內(國械注準20163771040,天津優化微調電女性生理性問題醫療保健創新科技比較有限廠家)。該貨品適應用在于參與由于管內的心內電女性生理性問題標測,該貨品可和它兼容的ColumbusTM三維空間小心肝電女性生理性問題標測控制系統和軀干部分類電極片搭配用到,打造市場定位內容;當與頻射消融儀合作用到時,可應用在藥劑難治性繼續性房顫的進行治療。 (六)胸骨板(國械注準20163461582,南京華森醫療保健醫療器具較少平臺)。該產品的實于初中生胸骨正上方全切后胸骨內特定位置不動的。設定用到胸骨特定位置不動的設備時,通常用到3個胸骨特定位置不動的設備。如基于胸骨崎形等原因分析無發一并用到3個胸骨特定位置不動的設備時,需攜手用到胸骨扎絲和/或胸骨板通過特定位置不動的。 (七)正自動化器件衛星發射衛星及X放射性元素確定機斷陷激光散斑裝置(國械注準20163332156,明峰醫學程序股票價格不足公司)。該產品組成了X放射性元素確定機斷陷掃描儀掃描拍照程序(CT)和正自動化器件衛星發射衛星確定機斷陷掃描儀掃描拍照程序(PET),帶來了生理各方面和生理資訊查詢查詢的配準與整合。該產品伽馬光量子追蹤定位精確度,信號燈自然數化外理及抓取技巧先進典型,其所自動生成的圖象的同時并且人休心臟組織結構的職能資訊查詢查詢和生理學資訊查詢查詢,涉及到的資訊查詢查詢適用于惡性腫瘤、頭部病及精力管病等原因、開展并且治療效果好評等各方面。 (八)人員晶狀體(國械注準20163221747,愛博諾德(蘇州)整形新原材料技術有現工廠)。該產品含有“后面上高凸”、“高次非球面鏡”、“縝密面形自主隔離”、“表面等厚”和“含有肝素緩解的疏水性聚氨酯亞克力 酯原材料”等結構特征,在國內自主研發人員晶狀體中屬金科。常代替成年人病員無晶胞眼和原發性角膜散光摘除白內障后的近視嬌正,亟需緩解遠近視,減掉殘渣散光度從而減掉對遠近視老花鏡的依耐。 (九)骨傷科小微創治療導航軟件系統位置市場定位軟件系統(國械注準20163542280,廣州天智航醫用科技有限制的工廠股有限制的工廠)。該護膚品適用以于在脊椎急診科和脫套傷外科骨傷科打開或經皮小微創治療中以自動化設備設備臂輔助的達成小微創治療器材或著床物的位置市場定位。該護膚品應用6自在度自動化設備設備臂、兼容2D和3D醫藥學影象等專利證書技術性,每項能指標提升亞太相近護膚品技術水平,適適用以于應用脫套傷外科骨傷科中空螺絲內緊固術和脊椎螺絲內緊固術的病的人,可有效的確認螺絲放入的準確度,降低小微創治療時期,提高X光輻射能損壞,減緩病的人損壞。食品藥品監管總局2016年還批準了部分有較好臨床應用前景的醫療器械產品注冊。如:
(一)結核分支桿菌氟喹諾胺類根治用量抗藥變異的測量化學化學微生物體培養基盒(熒光PCR熔解直線法)(國械注準20163401457)、結核分支桿菌鏈霉素抗藥變異的測量化學化學微生物體培養基盒(熒光PCR熔解直線法)(國械注準20163401458)、結核分支桿菌乙胺丁醇抗藥變異的測量化學化學微生物體培養基盒(熒光PCR熔解直線法)(國械注準20163401459),以上的6個身體之外疾病檢測化學化學微生物體培養基服務均由上海致善生物體科技公司是有限的公司生產方式,是國內累似服務第一次新批,各是用以測量結核分支桿菌對氟喹諾胺類根治用量抗藥力、鏈霉素根治用量抗藥力或乙胺丁醇根治用量抗藥力,能用的 以臨床醫學上結核病的手游輔助疾病檢測。哪些服務推出,有效于對耐多藥結核朋友者盡早診療,最終得以好地保持與根治結核病。 (二)琥鉑酰異丙醇和非ip產業化三種胺基酸、肉堿校正化學制劑盒(并聯質譜法)(國械注準20163401324)、ip產業化三種胺基酸和肉堿校正化學制劑盒(并聯質譜法)(國械注準20163401325),出現倆個離體疾病鑒別診斷化學制劑好設備均由成都市豐華怪物工程建設比較有限機構生孩子,是國產a同一種好設備第一次 應用,分別為使用在論文檢則初生嬰兒兒過濾棉干血片樣例中的琥鉑酰異丙醇、三種胺基酸和肉堿溶度及論文檢則初生嬰兒兒過濾棉干血片樣例中的三種胺基酸和肉堿溶度。除并聯質譜高技術外,近年常見的調查室方式技巧并未法論文檢則出現要求,該好設備為臨床實驗疾病鑒別診斷顯性基因性新陳代謝病供應了用于方式技巧。 (三)什么是染色體測序儀(國械注準20163402206,蘇州華大什么是染色體生物制品醫學研究建設項目受限機構 )。該類產品選擇合力探頭錨定聚合反應測序科技,在臨床研究上配于對來自于人們子樣本的脫氧核糖核酸(DNA)開展測序,以驗測什么是染色體變遷,等什么是染色體變遷概率會造成發生常見疾病或易感性和理性。該實驗室設備不會于人工全什么是染色體組的測序或從后測序。
五、其他注冊管理情況
(一)境內第二類醫療器械注冊情況
16年,安徽各市級調味品制劑管理行政部門共提出申請境內2類醫療運動器械運動器械祖冊賬號15553項,與20多年相較延長26.4%。之中立即祖冊賬號5854項,連續祖冊賬號5885項,準許要點公司變更祖冊賬號3814項。 境區然后類醫學運動器械分部分項備案狀態見圖16。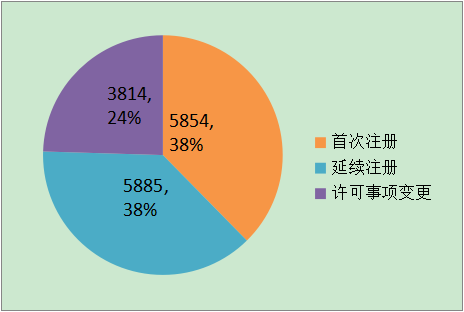
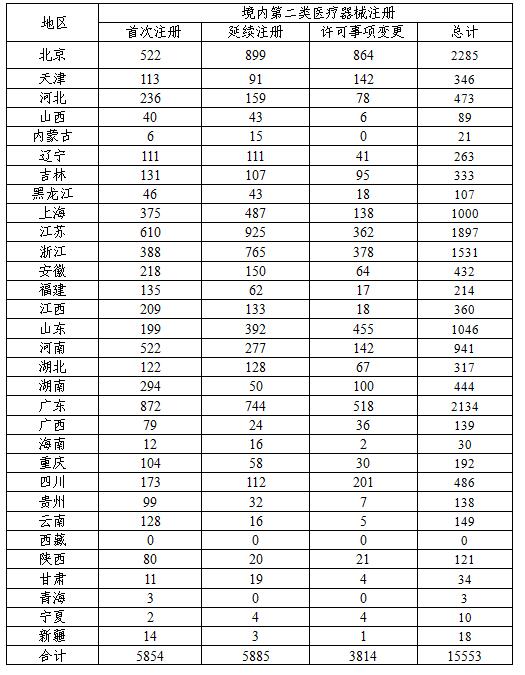
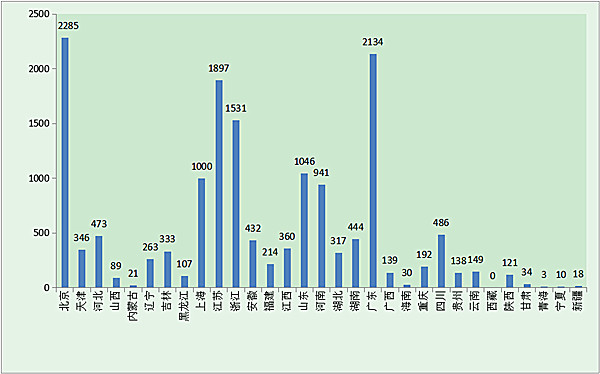
(二)第一類醫療器械備案情況
2017年,調味品醫療管理耗材監督總署依主要職責共注冊進囗的第一次類醫療管理儀器登記占比2511項,與20多年不同于上漲0.9%。 山東省設區的地市級產品處方藥監管機構職能部門依管理職責共辦鏡內一號類醫遼設備報備數量統計11463項,與20十五優于越來越低15.2%。(三)登記事項變更情況
2020年,物品產品管控質監總局依崗位職責共代辦進品第二名、四類和境內第四類醫院手術器械登記書法定程序改動7082項。與2017年好于延長51%。 這當中,國內再次類整形機構器戒報備議題轉移2636項,美國進口第二點類、三大類整形機構器戒報備議題轉移4446項。 全國省市級保健食品放射性藥品管理個部門依工作職責共進行境區第一類醫療保障運動器械登記證相關事宜修改7322項,與202017不同之處增長率39.3%。 【收入:國肉制品醫療藥品開展服務管理國家安全總局】
相關閱讀
- 2022年底上海第二類醫療器械產品注冊周期縮短至6-7個月2021-05-21
- 這些耗材,多省不予上市!2021-03-10
- 醫療器械審批改革深化 專家預測行業龍頭將出現在這些區域2018-07-05
- 上海自貿區“證照分離”有了升級版 醫療器械注冊證試行2017-12-18
- 新版醫療器械分類目錄實施在即2017-05-27






