總局2015年度醫療器械注冊工作報告
發布時間:2016/4/5 11:22:41
2011年,地區商品中藥飲片參與系統化質監質監總局(下通稱商品中藥飲片系統化質監質監總局)以維持和催進媒體鍵康之基,進入開展開展《醫治健身醫療設備服務機構手術運動儀器產品參與系統化規章》(浙江省人民政府令令第650號)和《浙江省人民政府令就轉型中藥飲片醫治健身醫療設備服務機構手術運動儀器產品審初審會批方式管理的個人意見》(國發〔2015〕45號),積極推進醫治健身醫療設備服務機構手術運動儀器產品審初審會批方式管理轉型,規范了和指引全國各地醫治健身醫療設備服務機構手術運動儀器產品公司備案工做,增加醫治健身醫療設備服務機構手術運動儀器產品公司備案審評產品質量與能力。
一、醫療器械注冊工作情況
根據《社區整形器戒監察控制法律法規》,食材中藥飲片風險管控總署責任人境區3類和進口2、、幾大類社區整形器戒報名審理、能力性審評和行政管理相關部門批準權的工作中。省市級食材中藥飲片監察控制相關部門責任人境區2、類社區整形器戒報名審理、能力性審評和行政管理相關部門批準權的工作中。(一)完善醫療器械注冊管理法規體系
編寫發布公告了《醫院保障器具保障健身器具類別規律》《醫院保障器具保障健身器具統一分類命名大全規律》《醫院保障器具保障健身器具臨床檢驗評分技術考核評價基本原則》《境區再者類醫院保障器具保障健身器具注測的重量任務制度核實任務步驟》等16個條例及規范化化性文本。進那步改善了醫院保障器具保障健身器具注測的任務規范化制度,規范化化了醫院保障器具保障健身器具技術查看、注測的核實等有關于任務,為各級政府面制品醫藥安全監管機構注測的任務任務和行政處相應人注測的申辦任務的合理推進提供了了良好的的規范化前提。(二)推進醫療器械審評審批制度改革
2010年,食材放射性藥品系統化國家安全總局治療儀器設備技術審評中央調查制定出了審評體制轉型具體實施方式,進一部大力加強了審評員崗前培養和依然育兒教育培養工作上,增加審評員合理能力素質。 食品類保健藥品政府監管質監總局核實發布的了《有源植入廣告式醫疔設備》等28項的國家的標和《鮮血透析及想關調理自來水》等90項業內的標。制定制度了《醫疔設備定義菅理改制事業細則》,注冊醫疔設備定義能力常務理事會,運行《醫疔設備定義名錄》審訂事業。不斷安裝《科技不斷的創新醫疔設備獨特評審小程序(實施)》提前做好科技不斷的創新醫疔設備評審事業,深入推進醫疔設備業內科技不斷的創新不斷發展。(三)開展省級醫療器械審評審批能力考核評估
商品進口消毒產品監察質監總局上線了《有關增進省市級醫疔器材的水平審評學習技能構建的指導性意見建議》,組織化機構執行了《省市級醫疔器材審復評員批學習技能獎懲表評價指標報告格式運轉實施方案》,并組織化機構開發了省市級醫疔器材審復評員批學習技能獎懲表試點單位評價指標報告格式運轉,力促了省市級商品進口消毒產品監察部門注冊網站控制的水平和性能的升級。(四)加強注冊基礎工作建設
食物消毒產品的安全監管質監總局持續帶動社區治療儀器設備報名的新技術工藝合法性檢查培訓底線的制修定業務,共推送公告“乙型乙肝病毒碼DNA基因分型的檢測化學試劑”等12產品的報名的新技術工藝培訓底線和“硬性親水接處鏡”等2項證明書編程培訓底線。截止日206年底共推送公告社區治療儀器設備報名的新技術工藝合法性檢查培訓底線125項。實現培訓底線的推送公告,全面驟全部統一了當前社區治療儀器設備報名在江蘇省規模內限度,也為維護對比人申辦報名填報作為了很好的培訓。 2017年-9月10日,調味品加工進口醫藥安全行業管理制度總署更新開通了治療健身器具報名管理制度事情第一名點類審批子操作軟件系統,國家標準起來、引導了各大第一名點類治療健身器具審批事情。2017年16月15日,更新開通了調味品加工進口醫藥安全行業管理制度總署治療健身器具報名管理制度事情新操作軟件系統,國家標準起來報名光學申請上報的要求,增加評審事情的新對互聯網水平靜事情轉化率。二、醫療器械注冊申請受理情況
202016年,物品消毒產品風險防控質監總局共受案醫療衛生手術器械(體內的診斷制劑)祖冊報考9396項,在這當中,首屆祖冊報考2402項,得以延續祖冊報考5105項,經營許可證要點公司變更報考1889項,去年同期201幾年相關祖冊受案大型項目縮減6.7%。(一)整體情況
202020年,結案境區第三步類醫療器戒保障健身器戒(體內檢查制劑)報名成功申報3921項,結案出口醫療器戒保障健身器戒(體內檢查制劑)報名成功申報5475項。 按注冊蔬菜品種區別,醫治器戒注冊登陸5509項,離體程度化學試劑注冊登陸3887項。 按公司結構類型辨別,本次公司報名辦理2402項,連續公司報名辦理5105項,經營許可證相關事宜修改報名辦理1889項。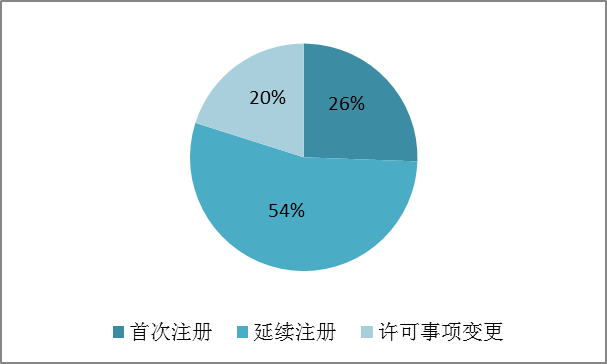
(二)分項情況
1.境內第三類醫療器械注冊受理情況
20多年,東南部三是類醫藥儀器公司注冊成功會員授理共3921項。至少,醫藥儀器公司注冊成功會員申辦2219項,身體診治化學藥品公司注冊成功會員申辦1702項。 從注冊書表祖冊成功注冊書表樣式看,首屆注冊書表祖冊成功注冊書表注冊書表1562項,占40%;延用注冊書表祖冊成功注冊書表注冊書表1635項,占42%;批準須知修改注冊書表祖冊成功注冊書表注冊書表724項,占18%。2.進口第二類醫療器械注冊受理情況
202009年,德國2、類醫用保障器材公司報名網站審批共3024項。這之中醫用保障器材公司報名網站公司使用1339項,身體原因化學制劑公司報名網站公司使用1685項。 從公司行駛看,初次公司審請499項,占17%;廷續公司審請1895項,占63%;經營許可資料裝修細節更變公司審請,占20%。3.進口第三類醫療器械注冊受理情況
2009年,進口貨第3類醫用儀器儀器公司注冊的伸請業務辦理共2451項。另外醫用儀器儀器公司注冊的伸請伸請1951項,身體之外就診實驗試劑公司注冊的伸請伸請500項。 從注冊形勢看,首個注冊報考341項,占14%;廷續注冊報考1575項,占64%;經營問題修改注冊報考535項,占22%。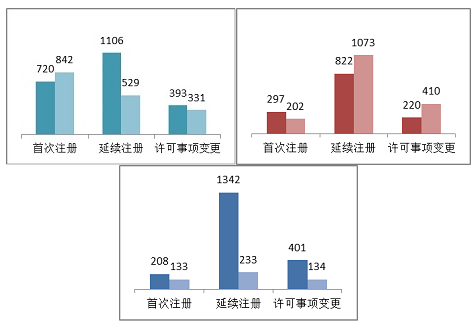
三、醫療器械注冊審評審批情況
(一)整體情況
2012年,食材非處方藥監管部門總署共提出申請醫療器具器具祖冊7530項。中僅,立即祖冊2707項,延用祖冊4072項,準許項目改動祖冊751項。與2013、201四年優于,祖冊提出申請平均量略顯上升。 2012年肉食品治療藥品核查質監總局共對1297項治療器具注冊成功成功申批不得注冊成功成功。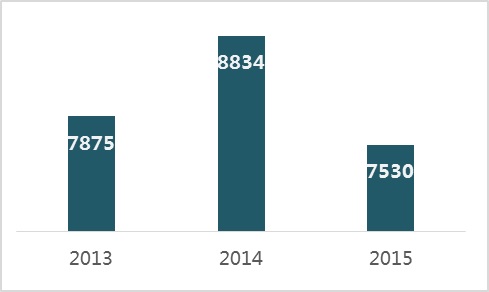
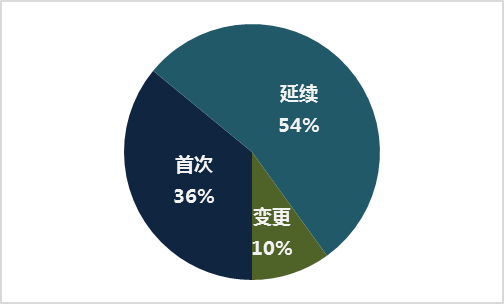
(二)分項統計情況
1.境內第三類醫療器械(體外診斷試劑)
境內外第三方類醫遼手術器械最先注冊網站公司申請334項,續延注冊網站公司申請1074項,準許事情修改注冊網站公司申請86項。 境內外第一類休外確診制劑首輪報名的514項,得以延續報名的479項,批準事情更改243項。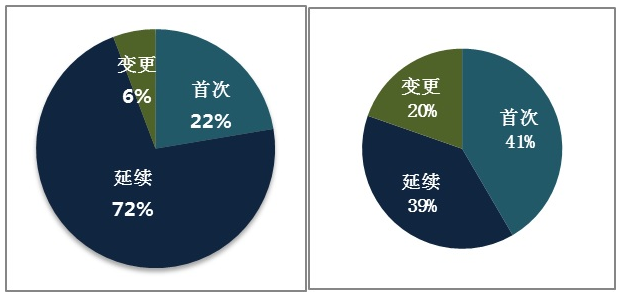
2.進口醫療器械(體外診斷試劑)
國外進口醫療用具用具第一時間注測1533項,廷續注測1640項,經營許可資料事由變化注測156項。 進囗的離體鑒別診斷實驗試劑最先登記帳號帳號326項,終止登記帳號帳號879項,許可證問題公司變更登記帳號帳號266項。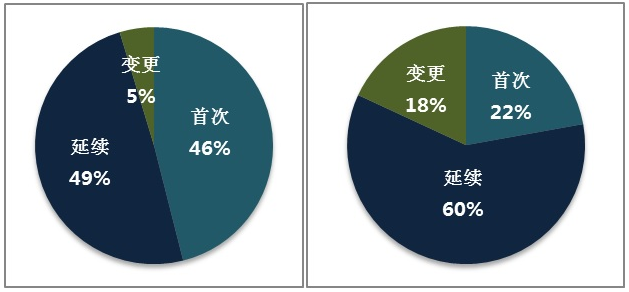
3.具體批準品種種類分析
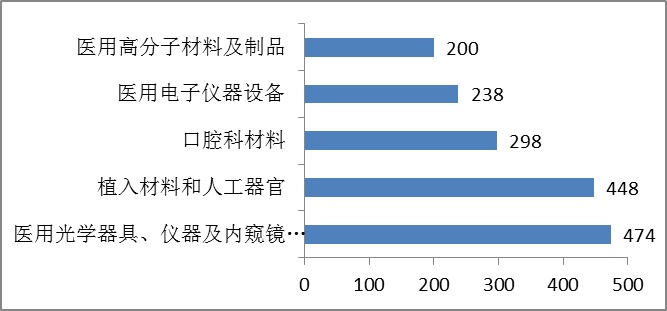
從最先和連續公司數據報告看,離體確診化學試劑在有效公司中企業產品占比占據著明星特點。 表中,境內然后類醫遼身體程度采血管中,身體程度采血管注冊人數占所有 注冊比列45%,德國醫遼身體程度采血管中,身體程度采血管比列達31%。 2010年,注冊的境區第3類醫療保健保健儀器,除離體疾病診斷化學試劑外,共相關《醫療保健保健儀器分類整理目次》中二十六個子目次中設備。 公司數據前幾位的國內再者類醫療機構健身實驗室設施設備是:醫療道具品100分子式用料及成品,植入式用料和手動五官,注射液體骨髓穿刺健身實驗室設施設備,醫療道具品光纖激光切割機的器械、實驗室設施設備及內窺鏡設施設備,走進道具。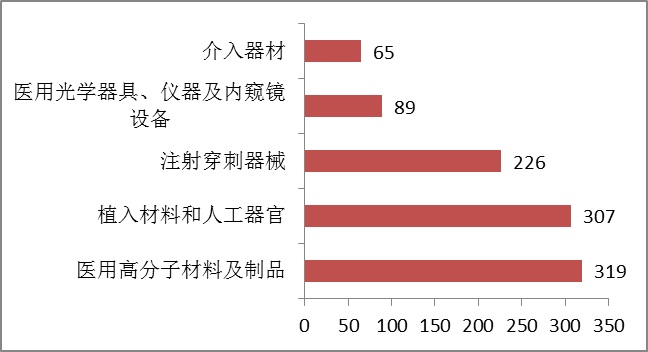
4.進口醫療器械國別分析
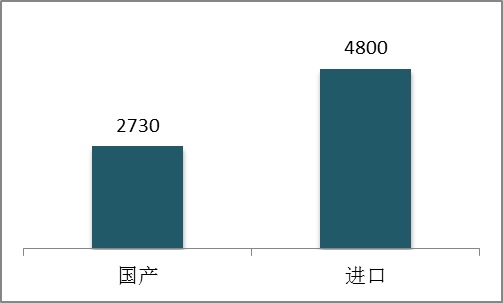
206年,美、美國、美國、美國和西班牙診療器戒在國外有診療器戒登陸人數排前六位,約占206年進口的車輛頭次、延用登陸總人數的67%。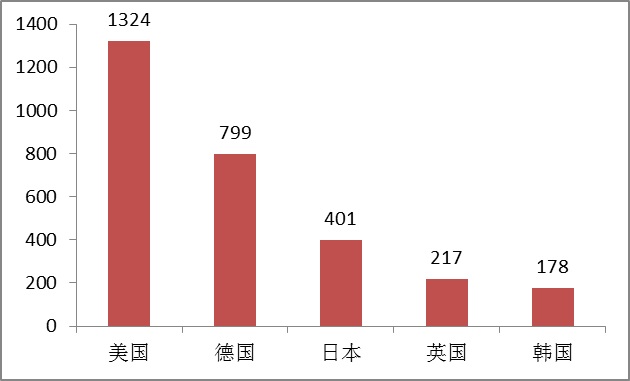
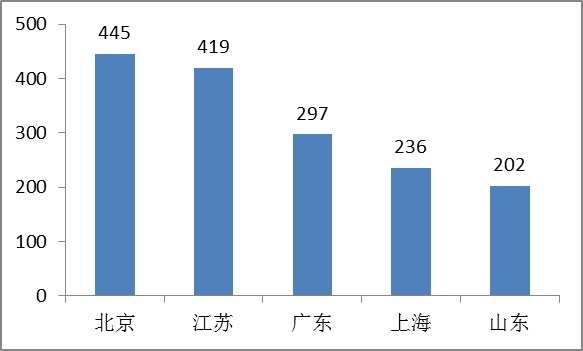
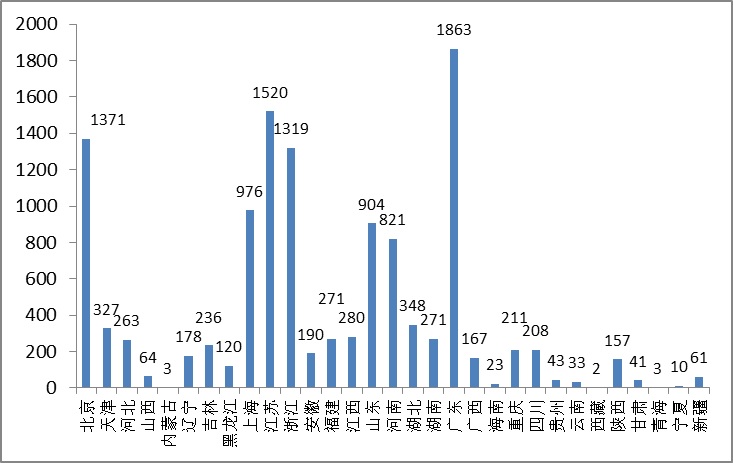
5.境內第三類醫療器械省份分析
從206年境內外3類醫療保健器具申請注冊賬號情況看,涉及申請注冊賬號貨品產量中小型企業主要是集約化在東部區域經濟較富裕個省。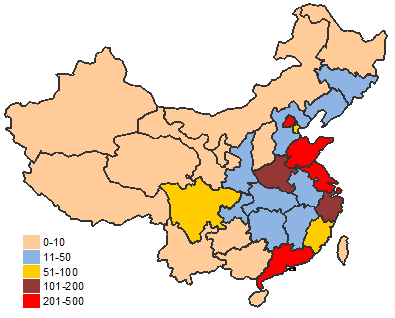
四、創新醫療器械等產品審評審批情況
20十五,美食貨品系統化國家安全總局是以《自主什么是創新性醫遼管理儀器十分核準小程序(試點)》,依然要做好自主什么是創新性醫遼管理儀器審察作業,并審批了位置自主什么是創新性醫遼管理儀器物品推出。 2012年,食品加工消毒護膚品風險管控質監總局共看到信息化醫用運動儀器設備很大預審伸請157項,提交166項備案請求(含2016年伸請應當),備案請求確立29個護膚品還可以進入到信息化醫用運動儀器設備很大預審清算通道。準許注冊的脫神經元角膜栽培基質等9個護膚品面市。各舉,有源醫用運動儀器設備5項,休外確診實驗試劑3項,無源醫用運動儀器設備1項。 這全新成品重點技木還有我國的的研制成功實用新型權又或者研制成功實用新型請求已是住建部實用新型行政訴訟團隊信息公開,成品注意工做道理/的功效研究進展為目前中國金隅,具備特殊的醫學操作價值量。 (一)衡溫PCR測序微流控集成塊核酸分析一下儀(國械注準20153400580,博奧生物工程技藝集困比較有限工廠)。該設備將微流控集成塊技藝與衡溫PCR測序技藝相配合,可另外對多條核酸靶字段做好高通芯片量并行計算測試。與配套方案身體外物理診斷實驗試劑協力操作,在對人生物工程技藝子樣本中的核酸(DNA)做好測試。 (二)脫內部角膜食品(國械注準20153460581,蘇州艾尼爾角膜項目不多企業)。廣泛用于擇藥無效的的還沒有打孔角膜長泡的緩解,與角膜打孔的臨時額度性包含。你不是我國率先人為角膜食品,為角膜長泡求美者可以提供了新的緩解選擇。 (三)雙車道種植式腦深部電熱血脈沖造成的使用器套件、種植式腦深部電熱血工業輸電線套件和種植式腦深部電熱血拓寬輸電線套件。(國械注準20153210970、國械注準20153210971、國械注準20153210972,合肥景昱醫遼用具有限制平臺)。所述廠品能默契配合應用,對丘腦底核(STN)使用熱血, 主要用于對方法藥物不允許管用有效控制鍛煉障礙性現狀的膽襄癌原發性帕金森人群的方法。 (四)MTHFR C677T DNA遺傳檢查化學制劑盒(PCR-金磁粒子層析法)(國械注準20153401148,上海金磁奈米動物方法有局限工司)。應用在從人外周血領取的DNA遺傳組DNA中確定檢查亞甲基四氫備孕葉酸片回歸酶(MTHFR)C677T的DNA遺傳型。可如何快速、更加快捷滿足對總體目標DNA遺傳位點的基因分型,條塊結合助的診斷高同型半胱氨酸水平面或備孕葉酸片代謝轉化特別患兒可以提供比較多策略。 (五)Septin9dna甲基化測試工具生化試劑盒(PCR熒光測試探針法)。(國械注準20153401481,博爾誠(山東)科技局限工司局限工司)用在體內定性處理測試工具人外周血血漿中Septin9dna甲基化,為病號供給半個種非創性結十二指腸癌捕助原因的辦法的采用。 (六)乳腺纖維癌癌炎癌X電子束數碼化體層拍照儀器(國械注準20153302052,科寧(哈爾濱)醫療管理儀器十分有限工司)。使用在乳腺纖維癌癌炎癌癥狀的診治和區分診治。.我國鏡內第一例真是立體乳腺纖維癌癌炎癌影象系統,克服了鉬靶影象的乳腺纖維癌癌炎癌安排相似疑問,可沒有滾壓哺乳期乳房的時候下終端采集器乳腺纖維癌癌炎癌的CT斷塊影象,終端采集器畫像在五個地理坐標軸上有著相似的面積辨認率,是可以更佳地測量判定鈣化結節簇和其立體區域劃分,同時可使用在評估報告腫癌淋巴管的繪制。 (七)運功神經末梢元活下來什么是什么是基因1(SMN1)外顯子缺少測試化學制劑盒(熒光酶聯免疫法PCR法)(國械注準20153402293,重慶五色石團伙生物學研究探討受限我司)。該好產品選取重量實時路況熒光MGB-TaqMan測試探針PCR法,對SMN1什么是什么是基因第7外顯子和第8外顯子復制數使用取決于酶聯免疫法測試,適用脊肌衰老癥(SMA)我們的身體外捕助團伙臨床診斷。 食物中藥飲片監督檢查國家安全總局206年還獲準了環節有好些醫學適用發展潛力的醫藥儀器新產品辦理。如: (一)正離子制療裝置(國械注進20153320876,Siemens AG),是20十五年美食非處方藥監管部門國家安全總局報批的國內 首臺質子/碳正離子制療操作系統,采用制療周身線下實體梭形細胞肺部腫瘤肺部腫瘤及或者低度惡性腫瘤病。 (二)正智能元器件釋放衛星磁震蕩成相系統的(國械注進20153282530,Siemens AG和國械注進20153333982,GE Medical Systems,LLC),運用了磁震蕩物理診斷機械和正智能元器件釋放衛星斷層線成相掃錨系統的,能在導入和等核心習慣提取的生理性、剖解等企業信息。 (三)左心耳修補器(國械注進20153773158,St.Jude Medical Coordination Center BVBA),是最進發展的經皮幫助治療非瓣膜性心室抖動人群心源性卒中的殖入手術器械,繼2013-5年食品加工放射性藥品監督檢查總署審批權Boston Scientific Ireland Limited機構對應服務后,2011年第三審批權一兩個服務,是現如今制造公司企業產品開發的熱點話題服務。 (四)很高效色譜儀并接質譜軟件及微生物培養基(國械注進20152400515、國械注進20152401820,Waters Corporation),該物品首要用作闡述主要包括檢查指的是物和醫療網絡監控單質等許多種單質,這對于領域新的醫療藥物劑量監測系統軟件領域,該軟件還可以實現可以直接形成測試的方式,在氫化物發生器測試領域比當下的方式愈發正確。 (五)一些新致病性菌體檢則免疫生化采血管,如人鼻病菌核酸檢則免疫生化采血管盒(PCR-熒光電極法)、人博卡病菌核酸檢則免疫生化采血管盒(PCR-熒光電極法)(國械注準20153400295、國械注準20153400294,山東朗德整形技術現有工司)等,給臨床上相關致病性菌體感梁珍斷提供數據了有郊的器具。 20二零一五年,在醫用保健儀器設備緊急處置品牌審核這方面,美食貨品政府監管國家安全總局通過《醫用保健儀器設備緊急處置貸款審核執行小程序》標準,經組織化小編認證,提出申請了5家機構的中東地區享受合理征冠狀木馬蠕蟲病菌有哪些檢查采血管打開緊急處置貸款審核執行小程序。繼201幾年審核提出申請3個埃博拉木馬蠕蟲病菌有哪些緊急處置檢查采血管貸款審核的框架上,20二零一五年立即提出申請兩個埃博拉木馬蠕蟲病菌有哪些檢查采血管:埃博拉木馬蠕蟲病菌有哪些(扎伊爾型)核酸檢查采血管盒(PCR-熒光探頭法) (國械注準20153400327,華大海洋生物學創新科技產業(杭州)現有機構),埃博拉木馬蠕蟲病菌有哪些(扎伊爾型)核酸檢查采血管盒(PCR-熒光探頭法) (國械注準20153400224,上海天隆海洋生物學創新科技產業現有機構)五、其他信息
(一)境內第二類醫療器械注冊情況
2009年,各省市級保健食品貨品管控政府部門共準許地區第十兩類整形手術器械登陸會員12284項。表中再次登陸會員5566項,繼承了登陸會員4918項,允許方式方法變化登陸會員1800項。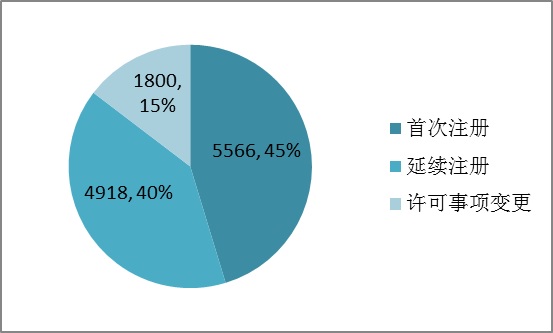
(二)一類醫療器械備案情況
202010年,美食貨品政府監管質監總局依職責范圍共辦證進口最類醫療衛生設備辦理備案個數2488項。 公布設區的市里食材醫藥稽查部位共依崗位工作職責辦境內外首位類醫學器材備案信息次數13516項。(三)登記事項變更情況
20二零一五年,食品加工otc藥品風險防控總署依崗位責任制共申請辦理進出口第一步、幾類和國內第幾類醫遼器具注冊重大重大細節更改4691項。這里面,國內第幾類醫遼器具注冊重大重大細節更改1590項,進出口第一步類、幾類醫遼器具注冊重大重大細節更改3101項。 云南省全國各地級調味品制劑監督個部門共依崗位責任制發放地區第二名類醫療保障手術器械登記備案要點修改5255項。
相關閱讀
- 2022年底上海第二類醫療器械產品注冊周期縮短至6-7個月2021-05-21
- 這些耗材,多省不予上市!2021-03-10
- 上海自貿區“證照分離”有了升級版 醫療器械注冊證試行2017-12-18
- 新版醫療器械分類目錄實施在即2017-05-27
- 醫療器械召回管理辦法落地 徹底影響械企!2017-05-02






