36家械商遭飛檢,27家查出問題,7家沒查成,1家已關門,還有1家...
發布時間:2016/9/2 14:50:16
我國國家國家藥監局局質監總局爭對醫療機構手術器械經驗制造業企業的航行查檢已經刺激性,部位國家國家藥監局局局卻就經行動計劃了。
昆明市國家藥品監督管理局局于二零一六年八月10日至12日對管區內36家社區醫療運動運動器械運動運動器械經驗企業做了航行檢測。該飛檢是要根據《介紹起草說明昆明市專項專項整治社區醫療運動運動器械運動運動器械調運業務領域經驗舉動做實施方案格式的通告》(洪食國家藥品監督管理局字〔2016〕130號)等的要而展平的,也即歸入械商大專項專項整治的一臺分。
飛檢關鍵字為25家營業速凍箱速凍產品設備的營業制造業工業企業和11家某些多種類型的醫療管理醫療器營業制造業工業企業,由南昌市市藥品監督管理局在各監督基層單位選擇了20名行政執股東員,成分10個飛檢組,使用別的地方討論會檢修的方式英文組織結構全面實施。
特別飛檢主要內容有4項:市場銷售經濟條件需不需要有與許可證書審核的時同步;想要冰凍箱、冰凍醫療服務運動器械的冷鏈物流管控需不需要有符合國家的規定;驗證的產品的需不需要有從正規靠譜產品的線采購;需不需要有留有市場銷售無注冊的證、突破高效期的產品的的這種現象等。
對這36家品牌的飛檢效果如表:
1、有1家之前就已經注銷了。

2、有7家質檢員沒能進入現場實施飛行檢查,原因幾乎都是,企業相關人員在外出差...
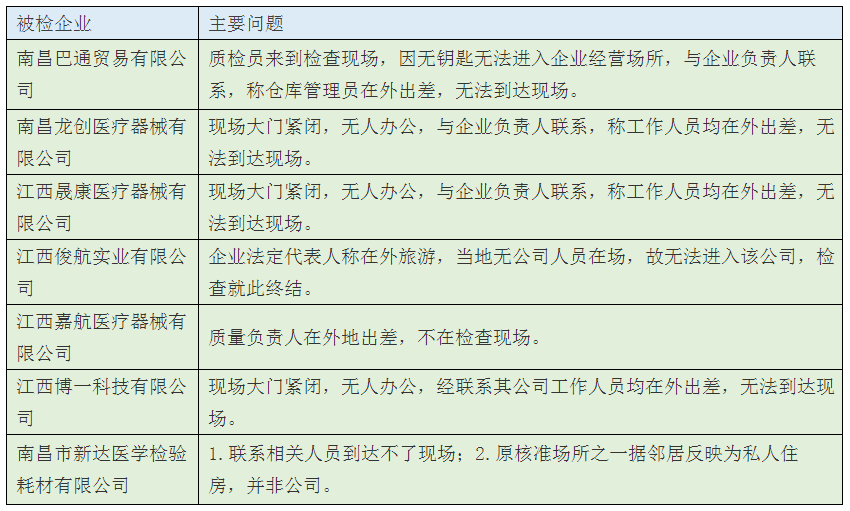
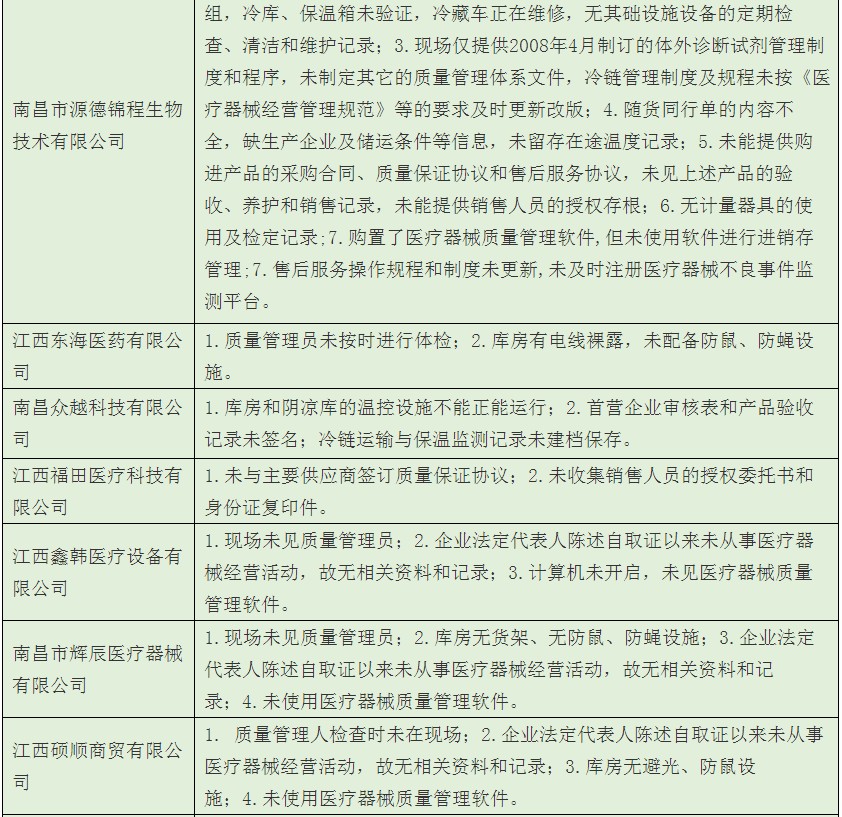
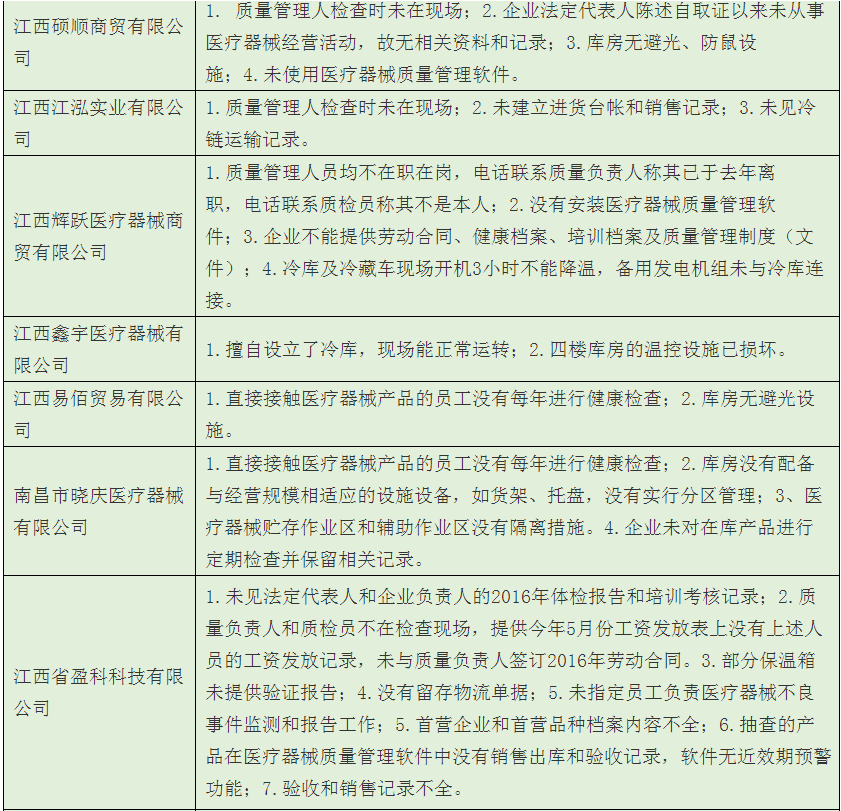
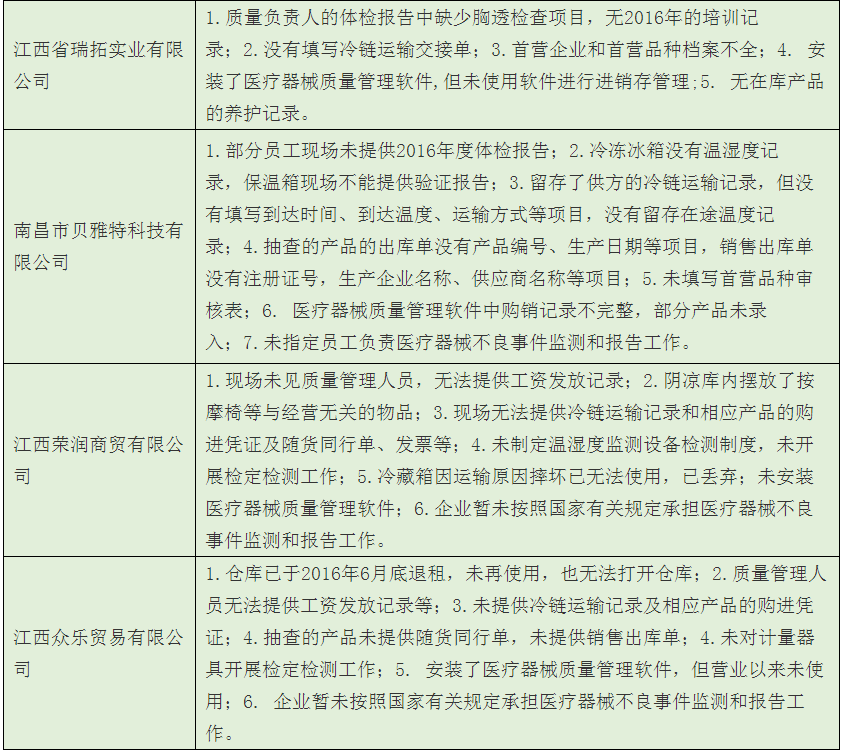
3、有27家被檢查出存在各種各樣、或多或少的問題。


4、還有1家企業,這是檢查了呢?還是沒檢查?


相關閱讀
- 國家藥監局司長:醫械企業飛檢不夠,將大力加倍!2018-09-11
- CFDA出手醫械:抽檢、飛檢、查翻新再售2017-02-20
- 國家飛檢6藥商被撤證!票據、掛證是重災區2016-11-01
- 2省開啟最嚴醫械臨床數據核查 3省造假處罰最嚴2016-09-29
- 進口醫械日常執法難題待解2016-09-28






