2017年將在美國上市的10大醫療設備
發布時間:2017/2/6 10:34:50
新的有一年有,也預示著連連串創新醫療器械衛生主系統將在意大利有。被寄托厚望的系統是指高血糖主系統、新形經軟管主動的脈瓣,并且創新做手術機子人體統。在這個盤點19年自身期望了解到的意大利10大醫療器械衛生主系統。
NO.1 波科公司的Lotus Edge

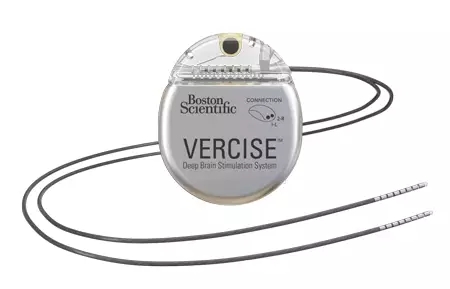
NO.2 波科公司的Vercise腦深部刺激系統
NO.3 強生公司的OneTouch Via

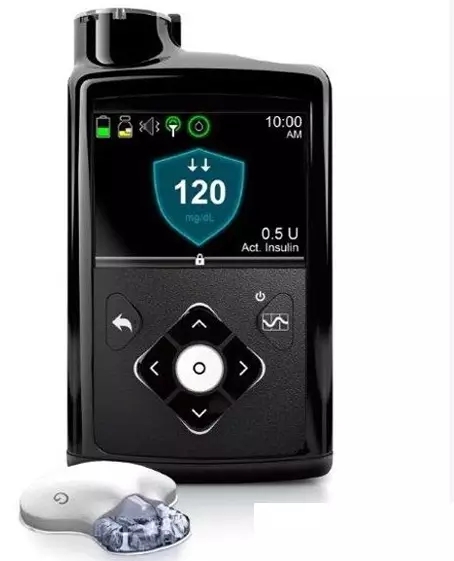
NO.4 美敦力的MiniMed 670G系統
NO.5 美敦力的Resolute Onyx藥物洗脫支架
藥品沖洗掉支吊架(Drug-eluting stent,DES)大頭美敦力集團盼望就可以在近日其中一個財年(4月底)收場前在芬蘭市面發布新聞Resolute Onyx DES。Resolute Onyx現在已經于201幾年15月賺取了歐洲國家CE注冊,2016二月增多了相關尺寸圖和融入癥。終止201八年5月4日,這牌車輛無權賺取芬蘭FDA監督政府部門的申批或信賴。 新的整年即將來臨,也意思著連下串新款診療生產體系將在USA出現。被寄于厚望的體系涉及到高血壓生產體系、新形經picc導管相互脈瓣,同時新款項目器機人體系。在這里盤存就在今年糖尿病患者期許找到的USA10大診療生產體系。NO.6 Neuronix Medical公司的neuroAD治療系統
NO.7 圣猶達公司的HeartMate 3左心室輔助系統

NO.8 圣猶達公司可用于磁共振的ICDs和CRT-Ds

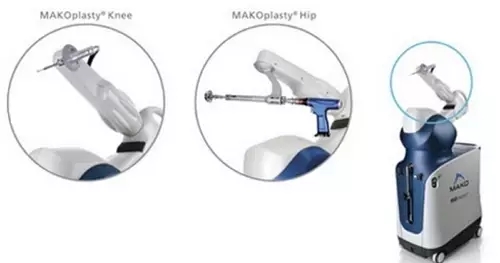
NO.9 史賽克用于MAKO系統的Triathlon全膝關節
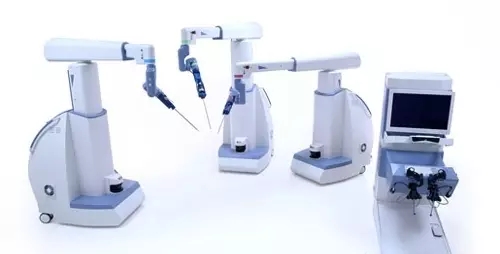
NO.10 TransEnterix公司的Senhance外科機器人系統

相關閱讀
- 國內血管介入手術機器人賽道迎來“黃金時段”2022-11-02
- 支氣管鏡手術機器人開啟肺部疾病診療賽道新篇章2022-03-02
- 最新排名出爐:2020全球頂級醫療企業TOP102021-02-05
- 21省耗材帶量采購:美敦力、雅培、微創、樂普…2021-01-14
- 知名械企分食170億市場:美敦力、史賽克、威高...2021-01-12






