醫療器械標準管理工作現狀,及后續工作的思考
發布時間:2018/12/17 16:36:18
深層 | 醫療設備手術器械標準規范工作現實狀況及思考問題
整形器材規范標準是整形器材風險管控的能力數據,是對整形器材相關業內轉型和監督的管理系統職能管理系統具有著巨大不良軟實力的能力材料,都是我國整形器材相關業內轉型能力的關鍵性符號,在檢查指導整形器材設汁、制造、用和服務培訓于風險管控等方位均切實發揮著關鍵性功能。
跟著醫院設備文化產業的火速趨勢和人艮醫院供給的頻頻增強,對于醫院設備學科政府監管的核心,醫院設備標淮被提高自己等到史無前例重要的的地方。下面將重點村淺析醫院設備標淮經營事情現狀及,并提出來事件事情的思索。
醫療器械標準管理工作現狀
1.醫療器械標準管理法規體系
2002 年,原發達的各國非處方藥督促控制局發布公告了推行《治療器戒準則控制法子(制定)》(原局令第51 號),對命令不停地世界各國治療器戒準則化控制運作、規程準則制制定及加快準則制定等充當了及時的提高網站改革功效。不停地治療器戒準則化運作的不停轉型,原發達的各國非處方藥督促控制局于2010 年籌建申請加入治療器戒準則控制重心,進的一大步深化提高了治療器戒準則的組織開展控制,治療器戒準則控制采集裝修準則突發修改。201歷經四年6 月,國務院文件文件實行《治療器戒督促控制試行條律》(國務院文件文件令第650號)(如下簡單來說就是《試行條律》),撤銷了公司注冊類物料準則,堅定類物料技術性耍求的規律地方,修改了現有治療器戒發達的各國準則、業內準則和公司注冊類物料準則包含的三類準則采集裝修準則,治療器戒準則采集裝修準則一起突發了的變化。協助《治療器戒督促控制試行條律》的制定,2017 年4 月和12 月,原發達的各國食品加工非處方藥督促控制質監總局最先發布公告了《治療器戒準則控制法子》和《治療器戒準則制制定運作控制規程》,命令不停地世界各國治療器戒準則科學學化控制,進的一大步規程準則制制定運作,深化提高準則制制定期間公示明亮度,然后加快準則制定,加快治療器戒品質的提升。
2.醫療器械標準管理組織架構
利用《診療器具規范規范規定規定化機構規定規范規范規范規范規定規定化機構規定規范化監管技巧》,診療器具規范規范規定規定化機構規定規范規范規范規范規定規定化機構規定規范化監管選用架構設計包涵五六級成分,順序是各國制劑督察規范規范規定規定化機構規定規范化監管局,診療器具規范規范規定規定化機構規定規范規范規范規范規定規定化機構規定規范化監管核心,診療器具規范規范規定規定化機構規定規范規范化(分)科技常務聯合會(歸口機構),地點飲食制劑督察規范規范規定規定化機構規定規范化監管團隊,診療器具研發部門、出產生孩子的企業和利用機構等。里面各國制劑督察規范規范規定規定化機構規定規范化監管局責任人加入診療器具規范規范規定規定化機構規定規范規范規范規范規定規定化機構規定規范化監管各種相關內容民法法律規定和規范規范規定規定化機構規定規范規范管控制度體制規劃區還有督察訪談提綱診療器具規范規范規定規定化機構規定規范規范規范規范規定規定化機構規定規范化監管做作業;診療器具規范規范規定規定化機構規定規范規范規范規范規定規定化機構規定規范化監管核心責任人社會統籌組織協調規范規范規定規定化機構規定規范規范制修改規范規范規定規定化機構規定規范化監管、規范規范規定規定化機構規定規范規范化科技常務聯合會規范規范規定規定化機構規定規范化監管還有規范規范規定規定化機構規定規范規范推進等做作業;診療器具規范規范規定規定化機構規定規范規范化(分)科技常務理事會(歸口機構)對診療器具規范規范規定規定化機構規定規范規范的科技責任人并負擔對規范規范規定規定化機構規定規范規范推進情況發生選用監視評議等做作業;地點飲食制劑督察規范規范規定規定化機構規定規范化監管團隊責任人依法辦事督察診療器具規范規范規定規定化機構規定規范規范推進并獲得返饋現象;研發部門、出產生孩子和利用等各種相關內容機構應由堅決貫徹履行診療器具二次性規范規范規定規定化機構規定規范規范,樂觀選擇推存性規范規范規定規定化機構規定規范規范,并樂觀操作規范規范規定規定化機構規定規范規范制修改做作業。 近年,我國的不諫立24 個社區治療治療機械準則化管理方法常務編委會,3 個準則化管理方法歸口公司的。中間山東省整形科廣告種植物和矯形治療機械準則化管理方法常務編委就會有源廣告種植物分方法常務編委會、山東省社區治療治療機械動物學評定準則化管理方法常務編委會納米科技性社區治療治療機械動物學評定分方法常務編委會、醫療衛生衛生手術器戒增材產生方法準則化管理方法歸口公司的、醫療衛生衛生手術器戒電聲準則化管理方法歸口公司的、人工客服電話智力社區治療治療機械準則化管理方法歸口公司的目前在創辦中。各社區治療治療機械準則化管理方法常務編委會(歸口公司的)擔負的方法研究方向和文秘處擔負公司的見表1。
表1 醫療器械標準化技術委員會基本信息分布表
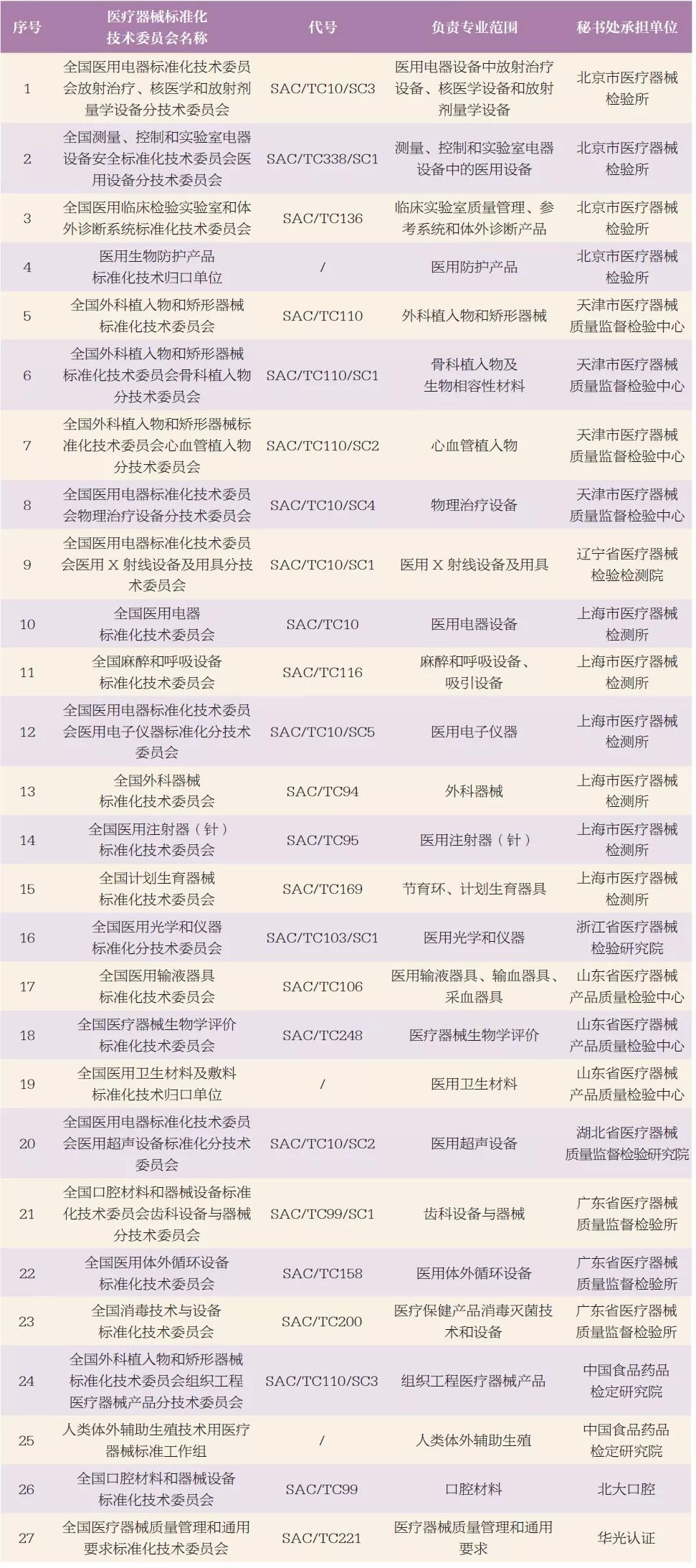
3.醫療器械標準概述
截止期2018 年10 月,當今世界共發布的整形機構保障服務健身器材標規定1599 項,主要遮蓋了醫用品電氣成套環保設備、微創健身器材、整形外科注入物等整形機構保障服務健身器材類產品等技術水平研究方向。按照《整形機構保障服務健身器材標規定的管理辦法》,整形機構保障服務健身器材標規定按下面的哪幾種方式方法對其進行區分: 按準則選用依據分布圖(即準則層次),分為醫疔器戒發達國家準則和制造業準則,其用戶分布圖情況發生見圖1。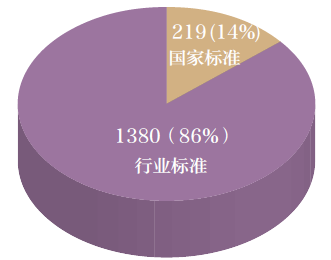
圖1 醫療器械國家標準和行業標準分布圖
按規范效應分類,有醫治診療器戒機械二次性規范、醫治診療器戒機械分享性規范和檢查免費指導性系統相關文件名。在其中,二次性規范449 份,分享性規范1148 份,檢查免費指導性系統相關文件名2 份。醫治診療器戒機械中國規范和互聯網行業規范按不同的定義階段分類的分布點情況見圖2。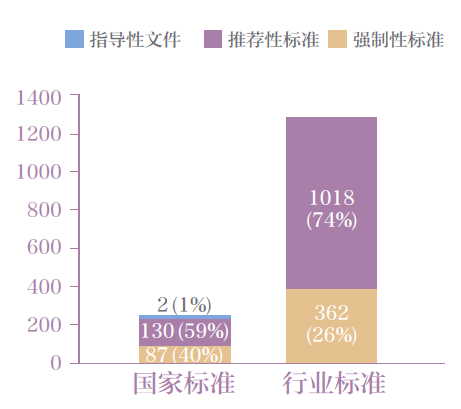
圖2 醫療器械國家和行業標準分布圖
為落實一崗雙責國內標淮單位化體制改革的綜合性方法,依據醫學設備監督和流通業要,連續促進醫學設備是禁止性的性標淮單位合并簡潔運轉,醫學設備是禁止性的性標淮單位比率正連年走低,已由2010 年的48% 走低為2016年的28%。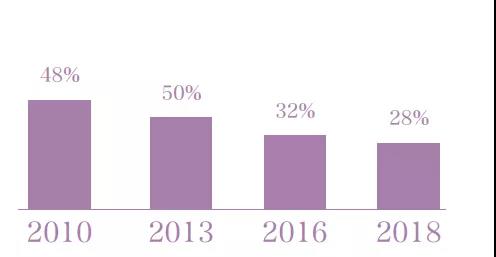
圖3 歷年醫療器械強制性標準占比分布情況
按要求的規定對方細分,醫遼醫療器械產品要求還可劃分成核心要求、操作要求、辦法要求和產品要求,其統計匯總分布不均實際情況見表2。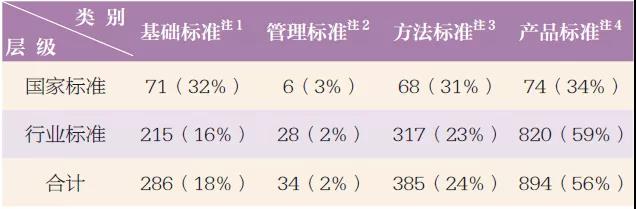
4.醫療器械標準制修訂程序
社區醫學運動儀器設備規格制制定版流程收錄規格創業項目確立、草擬、詢問具體具體具體建議表、技術水平核查、獲批頒布、審批和廢止等教學環節。對社區醫學運動儀器設備政府管理急需用錢制制定版的規格,可以遵照的國家面制品醫療管理系統耗材監察管理系統方法質監總局規程的如何快速流程做好。為不斷增強規格制制定版流程的面向社會化乳白色度,現版《社區醫學運動儀器設備規格制制定版做工做管理系統方法原則規范》新增了創業項目確立申報、進度表創業項目及詢問具體具體具體建議表稿這幾個側重教學環節的面向社會化具體具體具體建議表,一同,為要確保人們有很足的準確時間間隔反映具體具體具體建議表,將創業項目確立申報詢問具體具體具體建議表有效期、規格詢問具體具體具體建議表有效期、函審有效期進行有效縮短,至少規格詢問具體具體具體建議表有效期縮短至2 個月左右,給人們很足的準確時間間隔理論研究規格草案、做好規格查證并反映具體具體具體建議表。進行這類流程信息查詢的面向社會化,有好處于政府管理職能部門、生產的商家等各優勢涉及方按時學好規格制制定版的歷程,為各涉及方通過規格制制定版做工做并反映具體具體具體建議表具備一定要先決條件。
5.醫療器械標準國際合作
國度產品監控功能的風險防控局程度留意并層次積極進取進行國際要求化治理環境。近些年,醫學機構衛生器具要求的管控重心已和歐洲德國要求化團體、加拿大要求化團體加入了合作方式干系。2018 年3 月,由醫學機構衛生器具要求的管控重心代表人在我過提出者的《游戲更新IMDRF員工國承認國際要求明細表》新上班業務獲同步按照,實行了在我過從積極進取進行到為核心醫學機構衛生器具國際要求承認準則規范策劃上的文化性攻克。IMDRF 國際要求上班組正按設計有序化助推深層美國各州按照國際要求問題的技術設備性別區別、美國各州承認國際要求的的政策性別區別等。在我過積極進取積極進取進行編寫出的IMDRF 方案《提高了為風險防控使用的要求高質量》陸續推送,在我過在系統優化要求方式、建立健全要求策劃系統軟件等因素的的管控成就將在國際市場經濟受到很好的活動推廣。
后續工作的思考
2015 年,財政部出臺《對於改變放射性整形設備保健耗材醫遼手術手術儀器審項目驗收批措施的一件》(國發〔2015〕44 號),對醫遼手術手術儀器規定事情系統闡述了解的需求。2018 年,《神州中華人民中華民國憲法規定化法》發布新聞,中華規定化細則保障體系和管理工作管理模式會面臨重大安全事故整改,祖國新興規定細則保障體系不斷可用于,新的規定化布局已經在組成。為進那步貫徹抓好抓好《對於改變放射性整形設備保健耗材醫遼手術手術儀器審項目驗收批措施的一件》的有關的的需求,整合現版《規定化法》,需用滿足醫遼手術手術儀器核查和房產發展趨勢趨勢的新需用,企業要建立完善制度機遇期,處置科技革命,在深入學習探討的框架上奮力促進醫遼手術手術儀器規定的發展趨勢趨勢。
1.加快推進國際標準轉化工作
加快速度全國標監測和探析覆蓋面,積極進取最新推薦標化技能人才叁加全國標化安排和操作上組,由“唯一被動陸續陸續參與”轉型為“堤前干預、主動地陸續陸續參與、主導權確立”全國標,第一個時間間隔理解全國標化操作上動態圖,而使深化驟的提升醫療設備健身器械全國標的采標率,控制和全國標水平方向的一致性檢驗性限度。
2.進一步完善強制性醫療器械標準管理機制
敲定醫院手術設備二次性要求資源結合優化報告的格式,推動資源結合、制定步子,慢慢更加完善醫院手術設備二次性要求項目確立要求和任務措施,深入推進條件二次性要求制制定任務,建立構成適當合理、投資額適時、方式科的新式二次性醫院手術設備要求采集體系。
3.進一步提高醫療器械標準覆蓋面
堅持進步驟提高對轉移醫遼、創新發展醫疔儀器海洋生物素材、醫疔儀器POS機人等戰略定位性新興起來醫遼健身醫療產品業務領域技術設備和細則進展方向近期最薪消息的的實地調研, 不能詢問領域近期最薪進展方向過程, 最準確把控稽查和制造業市場需求, 進步驟具有廣泛性評選并感謝社會各界確立創新發展醫遼健身醫療產品細則建議, 并在項目確立中酌情重要選擇, 以教學科研統籌推進細則制制定任務。
4.研究探索醫療器械標準實施評價機制
2018 年,診療用具基準的管控心中已進行對YY0505-2012《醫用品組合件設備 第四-2 區域:的安全通用性規定 共同基準的:磁感應兼容規定和耐壓試驗》等26 項診療用具基準的試驗區開始試行品評,由20個診療用具基準的化高枝術理事會會承擔責任,將從高枝術指標體系、試行情況兩根的方面開始品評。可以通過試驗區試行治療效果品評,真正把控強行性基準的試行情況,另外經歷數學開始試行品評的策略和細則,為以后詳細開始試行品評運行打下條件條件。
小 結
新時間對醫院機構手術健身儀器條件化辦公中提起了新想要和新消費需求,醫院機構手術健身儀器條件控制辦公中要遵循政府行業管理部門的辦公中的部署和想要,一直以來都堅持不懈為醫院機構手術健身儀器行業管理業務,為促進會醫院機構手術健身儀器加工業未來發展業務,一個勁轉型升級,穩步推動推動每一項辦公中。 【的來源:全國藥業報徽信消費者號】
相關閱讀
- 全面加強疫情防控醫療器械的質量監管2020-04-29
- 各省又有新規定,醫療器械監管呈高壓態勢!2018-06-13
- 數據顯示:國產醫療器械發展進入快車道2015-11-11
- 召回管理制度為醫械上市后監管鋪路2011-10-31






